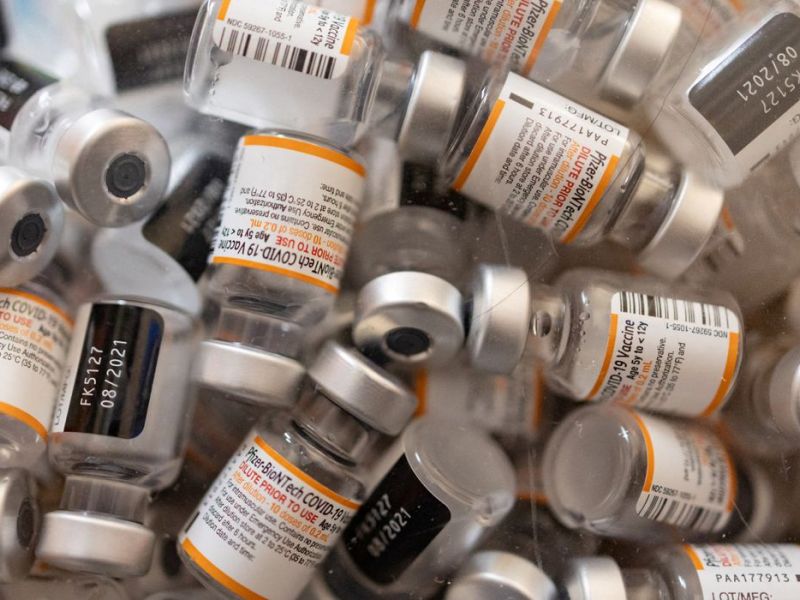
As farmacêuticas Pfizer e BioNTech disseram, nesta segunda-feira (23), que três doses de sua vacina contra a covid-19 geraram forte resposta imune em crianças menores de 5 anos, em ensaio clínico.
As empresas afirmaram que a vacina é segura e bem tolerada pelas crianças e que planejam, em breve, pedir aos reguladores globais que autorizem o imunizante para a faixa etária na qual nenhuma vacina está atualmente aprovada na maior parte do mundo.
Elas esperam concluir o envio de dados à Agência de Alimentos e Medicamentos (FDA) dos Estados Unidos nesta semana.
A Pfizer e a BioNTech disseram que três doses de uma formulação de 3 microgramas de sua vacina geraram resposta imune semelhante em crianças de seis meses a menos de cinco anos, em comparação à faixa de 16 a 25 anos que receberam duas doses da formulação de 30 microgramas da vacina em ensaio clínico anterior.
"O estudo sugere que uma dose baixa, de 3 microgramas de nossa vacina, cuidadosamente selecionada com base em dados de tolerabilidade, fornece às crianças alto nível de proteção contra as recentes cepas da covid-19", disse o presidente executivo da BioNTech, Ugur Sahin, em comunicado.
Segundo as farmacêuticas, uma análise inicial de 10 casos sintomáticos de covid-19 identificados até 29 de abril, enquanto a variante Ômicron era dominante, sugeria eficácia da vacina de 80,3% na faixa etária menor de cinco anos. Esta análise não é conclusiva, pois o protocolo do estudo especificou que a eficácia deve ser calculada com base em pelo menos 21 casos.
A Pfizer e a BioNTech disseram que os dados finais de eficácia na faixa etária serão compartilhados quando estiverem disponíveis.
Os 1.678 participantes do estudo receberam sua terceira dose pelo menos dois meses após a segunda. A Pfizer disse que a vacina foi bem tolerada, com a maioria dos efeitos colaterais adversos sendo leves ou moderados.